Prof. Dr. med. Klaus-Peter Hunfeld: INSTAND e.V. Vorstand - Stellv. Vorsitzender & Ringversuchsleiter
Zentralinstitut Labormedizin, Mikrobiologie und Krankenhaushygiene, Krankenhaus Nordwest, Frankfurt am Main
Seit der Einführung der Henle-Koch´schen-Postulate in die mikrobiologische Diagnostik 1882 gilt der direkte Nachweis von Erregern als Goldstandard in der Diagnostik infektiöser Erkrankungen. Mit der Entdeckung der Gruber-Widal-Reaktion vor nunmehr rund 150 Jahren (Abb. 1) wurde dann auch die infektionsserologische Erregerdiagnostik begründet. Heute sind eine große Zahl verschiedenster serologischer Testmethoden für den indirekten Nachweis von Bakterien und Viren im mikrobiologischen Routinelabor etabliert. Es war der Wiener Wissenschaftler Max von Gruber der erstmals den serologischen Nachweis von Antikörpern aus Seren infizierter Tiere und Patienten mittels Agglutination von Salmonella Typhi- und Vibrio cholerae-Bakterien für die Diagnose infektiöser Erkrankungen nutzte. Die gleiche Beobachtung wurde davon unabhängig später auch durch Fernand Widal 1897 beschrieben. Seither bleibt die Detektion erregerspezifischer Antikörper mittels immunologischer Methoden trotz der großen Fortschritte moderner molekularbiologischer Assays für den direkten Erregernachweis ein wesentlicher Pfeiler für die Diagnostik von Krankheitserregern aus Blut und Liquor.
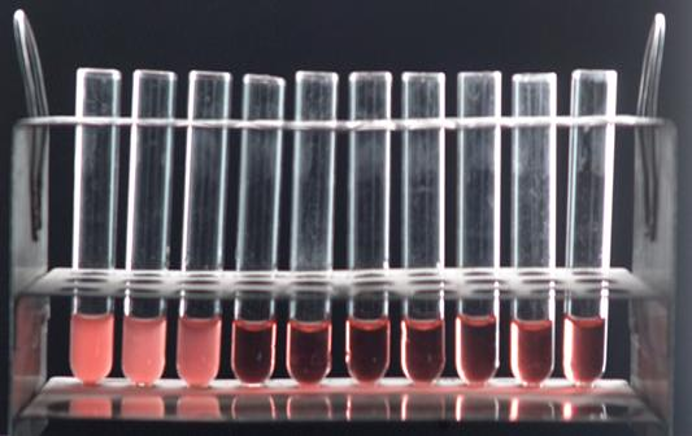
Abb. 1: Gruber-Widal Reaktion im Röhrchen
(Quelle: http://old-www.path.cam.ac.uk/Immunology/I_07.jpg)
Neben der grundsätzlichen medizinisch historischen Bedeutung dieser Entdeckung wird die sogenannte Gruber-Widal Reaktion bis heute in der Infektionsdiagnostik, insbesondere zur Diagnose von Folgeerkrankungen, bei Typhus und Yersiniose angewandt. Eine weitere bahnbrechende Entdeckung stellt die Entwicklung der Komplementbindungsreaktion durch Bordé und Gengou 1901 dar. Auch wenn heute Komplementbindungsreaktionen generell als nicht mehr akkreditierbar gelten, so stellen sie in vielen Laboratorien weltweit doch immer noch eine hilfsweise etablierte Methode dar, um insbesondere Infektionen durch seltene und schwer anzüchtbare Erreger mit relativ einfachen Mitteln zu diagnostizieren. Die Fortentwicklung dieser Methode durch August Paul von Wassermann und ihre Adaptation 1906 als schnelle und breit verfügbare Technik zur Diagnostik der Syphilis zählt ebenfalls zu den Meilensteinen bei der Etablierung von infektionsserologischen Tests im klinischen Labor.
Auch wenn derartige Techniken heute vor allen Dingen von medizinhistorischer Bedeutung sind, so sind die in ihrer Nachfolge entwickelten teil- oder vollautomatisierten immunologischen Testmethoden bis heute für die Detektion erregerspezifischer Antikörper und Antigene aus dem medizinischen Labor nicht wegzudenken. Diese Methoden benutzen eine Vielzahl von Abwandlungen von Antigen- und Antikörperreaktion unter Zuhilfenahme unterschiedlichster Reagenzien und Techniken und stellen in ihrer weltweiten Präsenz und Verfügbarkeit einen sehr lukrativen Markt für die Diagnostikaindustrie dar. Dabei sind diese Methoden trotz aller Bemühungen um Standardisierung nach wie vor von ganz unterschiedlicher Qualität und Verlässlichkeit, gerade wenn es um die zuverlässige Diagnostik von Infektionskrankheiten geht. Der klinisch diagnostische Anspruch den Beweis oder den Ausschluss bestimmter infektiöser Krankheitsbilder mittels dieser diagnostischen Techniken zu führen, bleibt, was eine transparente Informationspolitik bezüglich Spezifität und Sensitivität dieser Testsysteme angeht, eine große Herausforderung.
Aus der publizierten internationalen Literatur zur Qualität bakteriologischer Infektionsserologie ist klar ersichtlich, dass hier trotz vielfältiger Bemühungen große Probleme mit der Teststandardisierung fortbestehen und es insofern weiterhin an einer guten Vergleichbarkeit von Testergebnissen für die verschiedensten Erreger mangelt. Die indirekte Diagnostik von bakteriellen Erregern durch serologische Assays hat den Vorteil, dass auch eine Immunantwort gegen u.U. schwer anzüchtbare oder langsam wachsende Mikroorganismen, die durch Kultur oder molekulare Methoden kaum erfasst werden können, detektiert werden kann. Allerdings ist es durch die Variabilität der Testergebnisse, insbesondere zu Beginn der der Beschwerdesymptomatik oder in der Verlaufsüberwachung, schwer gut vergleichbare signifikante Testwertänderungen mit den verschiedenen Testsystemen zu erzielen. Auch sind gerade bei diesen Erregern die Befunde in der frühen Phase der Infektion noch negativ. Ein positiver Nachweis bestätigt eindeutig, dass es im Wirtsorganismus zu einer immunologischen Auseinandersetzung mit dem entsprechenden Pathogen gekommen ist. Allerdings muss in vielen Fällen offenbleiben, ob es sich dabei tatsächlich um eine akute Infektion oder aber, wie häufig zu beobachten, um eine durchgemachte Erkrankung mit einer serologischen Restantwort (Seronarbe) handelt. In gleicher Weise lassen sich allein aus serologischen Ergebnissen nur selten klare Aussagen zur Behandlungsbedürftigkeit oder zum Therapieerfolg im Verlauf ableiten.
In den tatsächlich bedeutsamen Indikationsfeldern der bakteriologischen Infektionsserologie, wie z.B. in der Diagnostik der Syphilis oder der Lyme Borreliose, lassen sich die o.g. Limitationen aber auch durch die Applikation moderner Kultur- und PCR-Verfahren zumeist nicht auflösen. Denn auch für diese Methoden und insbesondere für die molekularbiologischen Verfahren bestehen je nach Erreger und Manifestation insbesondere große Probleme mit der Sensitivität der Nachweisverfahren fort. Dies gilt umso mehr für viele der schwer nachweisbaren Pathogene in der Parasitologie, Mykologie und Virologie, so dass in vielen routinediagnostisch ausgerichteten medizinischen Laboratorien der Rückgriff auf infektionsimmunologische Nachweisverfahren derzeit alternativlos ist. Die häufig berichtete mangelhafte Qualität und schlechte Vergleichbarkeit immundiagnostischer Assays zum mikrobiologischen Erregernachweis resultiert nicht unerwartet aus der mangelhaften regulatorischen Anstrengung der Zulassungsbehörden in den vergangenen Jahren. Die neu aufgelegte IVDR versucht hier gegenzusteuern, schießt jedoch durch die inzwischen hochgesteckten Erwartungen und Anforderungen an für den europäischen Markt zugelassenen Diagnostika über das Ziel hinaus. Viele Hersteller kommerzieller Assays fürchten den hohen regulatorischen Aufwand und die nicht unerheblichen Investitionen für die Zulassung von Assays gerade für seltene oder schwer diagnostizierbare Erreger. Unter dem Druck der neuen regulatorischen Forderungen wurden und werden sogar eine ganze Reihe von bisher verfügbaren Diagnostika vom Markt genommen. Diese Problematik einschließlich der mangelnden oder einfach nicht transparent evaluierten Qualität von infektionsserologischen und hier insbesondere von bakteriologisch-infektionsserologisch ausgerichteten Testsystemen unterstreicht die dringende Notwendigkeit und die große Bedeutung der externen Qualitätskontrolle im Rahmen der durch die Richtlinie der Bundesärztekammer vorgeschriebenen regelmäßigen Ringversuche und ähnlicher Maßnahmen. Dies beinhaltet eine unabhängige Evaluation von Tests über das Repertoire der in der RiliBäk abgebildeten Parameter in E2 hinaus. Ohne entsprechende Ringversuche und deren transparente Auswertung und publikatorische Darstellung (Abb. 2 und 3) ist eine vernünftige Auswahl von Assays im Routinelabor und eine Abschätzung von deren diagnostischer Qualität praktisch nicht möglich. Dennoch ist es unabdingbar, dass auch unter dem Einfluss der neuen IVDR zukünftig zugelassene Assays klinisch besser evaluiert und in größer angelegten Zulassungsstudien auf Herz und Nieren geprüft werden, bevor sie dann auf den europäischen Markt gelangen. Die abgestimmte und gemeinsame Durchführung von externer Qualitätssicherung und einer guten klinischen Evaluation müssen Hand in Hand gehen, um in der Zukunft zu deutlichen Verbesserungen in der diagnostischen Qualität, der Vergleichbarkeit von Tests und der Beurteilung und Aussagekraft von Testergebnissen im klinischen Alltag kommen zu können.
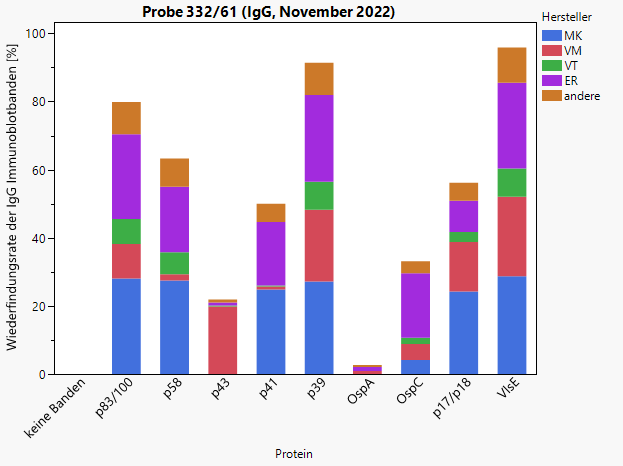
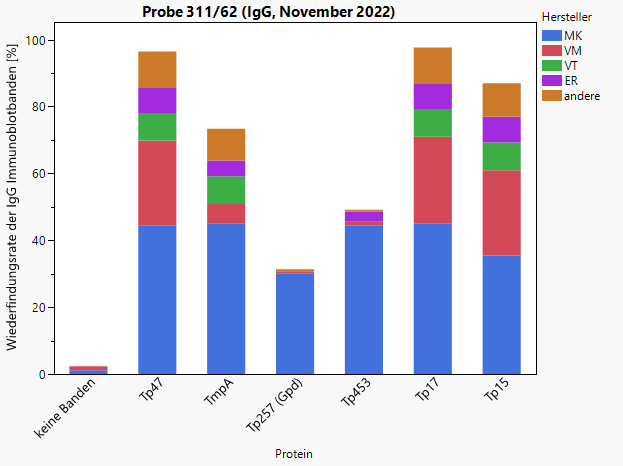
Abb. 2 und Abb. 3
Literatur:
Wellinghausen N, Abele-Horn M, Donoso Mantke O, Enders M, Fingerle V, Gärtner B, Hagedorn J, Rabenau H F, Reiter-Owona I, Tintelnot K, Weig M, Zeichhardt H, Hunfeld KP. (2018) MiQ, Immunological Methods for the Detection of Infectious Diseases. INSTAND e.V., Düsseldorf in Kooperation mit dem Dustri-Verlag Dr. Karl Feistle, Oberhaching, ISBN 978-3-87185-518-4.
Wellinghausen N, Abele-Horn M, Donoso Mantke O, Enders M, Fingerle V, Gärtner B, Hagedorn J, Rabenau H F, Reiter-Owona I, Tintelnot K, Weig M, Zeichhardt H, Hunfeld KP. (2016) MiQ 35, Qualitätsstandards in der mikrobiologisch-infektiologischen Diagnostik: Infektionsimmunologische Methoden. Urban & Fischer München, Jena.